結合の間合い
Servier社によるKEAP1阻害剤の報告。2-スルホニルチアゾールがwarheadとしてKEAP1のCys151残基と共有結合を形成する。3,000以上のオフターゲットタンパク質を評価して2つしか結合しなかった高選択性を持つが、これはwarheadの反応性が低く、複合体を形成 (化合物が標的タンパク質に結合)してCys/Serが近傍にないと反応しづらいためと思う。また、Julia-Kocienski試薬に構造が似ており、アクリルアミド付与以外に骨格に共有結合性を付与するデザインも可能かもしれない。
オレはこの間合いで十分・・・!!(つーか これが限界)

Covalent Inhibitors of KEAP1 with Exquisite Selectivity
J. Med. Chem. 2024, 67, 21208–21222.
https://doi.org/10.1021/acs.jmedchem.4c02019
KEAP1はE3リガーゼ複合体のアダプターとして、転写因子NRF2をユビキチン化し、プロテアソームを介して分解を誘導する。
NRF2は、抗酸化タンパク質の発現を調節するため、その活性化は自己免疫疾患や慢性腎臓病、神経変性疾患などの治療に期待できる。
NRF2の活性化は、KEAP1に結合し、KEAP1-NRF2相互作用を阻害することでNRF2の分解を抑制するアプローチが取られる。2013年にFDAによって多発性硬化症の治療薬として承認されたフマル酸ジメチルは、KEAP1の複数のシステイン残基と共有結合してNRF2を活性化する。フリードライヒ運動失調症治療薬として2023年に承認されたオマベロキソロンや、協和キリンが糖尿病性腎臓病やアルポート症候群を対象として開発していたバルドキソロンメチル (2023年開発中止)も、フマル酸ジメチルと同様のメカニズムでKEAP1のCys151残基との結合を介して作用する。
共有結合性阻害剤の主な懸念は、他の細胞内タンパク質に対する選択性であり、治療マージンを損なう可能性がある。そこで、Servier社は、選択性の高い共有結合性KEAP1バインダー(KEAP1-NRF2相互作用阻害剤/NRF2活性化剤)の創出を試みた。
【ヒット化合物取得および誘導体展開で化合物23取得】
①ヒット化合物の取得
・19万化合物ライブラリーでスクリーニング実施
✓1stスクリーニング:FRET β-lactamase reporter assay (NRFのARE結合)
✓2ndスクリーニング:complementation assay (NRF2の細胞核移行)
→両アッセイで単回評価後 (10 μM)、用量反応試験により162化合物取得
✓SPRで結合確認および細胞毒性評価により50化合物取得
・KEAP1の共有結合化合物1および2を選抜
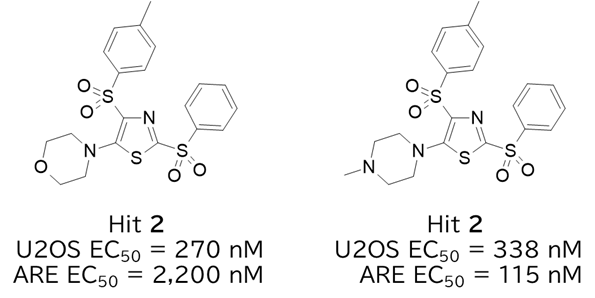
②化合物2の誘導体展開
・化合物2のピペラジンをピペラジノンに変換
✓化合物3は活性向上したが、ミクロソーム代謝安定性が低い
・化合物3のチアゾール2位のフェニルスルホニル基をエチル基に変換
✓化合物5は活性ほぼ同等で、ミクロソーム代謝安定性が改善
・化合物5のチアゾール4位のトルエニルスルホニル基を探索
✓脂溶性置換基を増やして疎水性を上げると活性向上するが代謝安定性低減
→活性と代謝安定性のバランスが良い化合物7を取得
・化合物7のチアゾール2位のエチルスルホニル基を再探索
✓小さいメチル基は活性向上したがt1/2が短くなっている
→化学反応性の増加による活性向上と推察
✓嵩高いcPr基やcBu基はt1/2が長くなったにも関わらず活性維持
→残念ながら代謝安定性低減
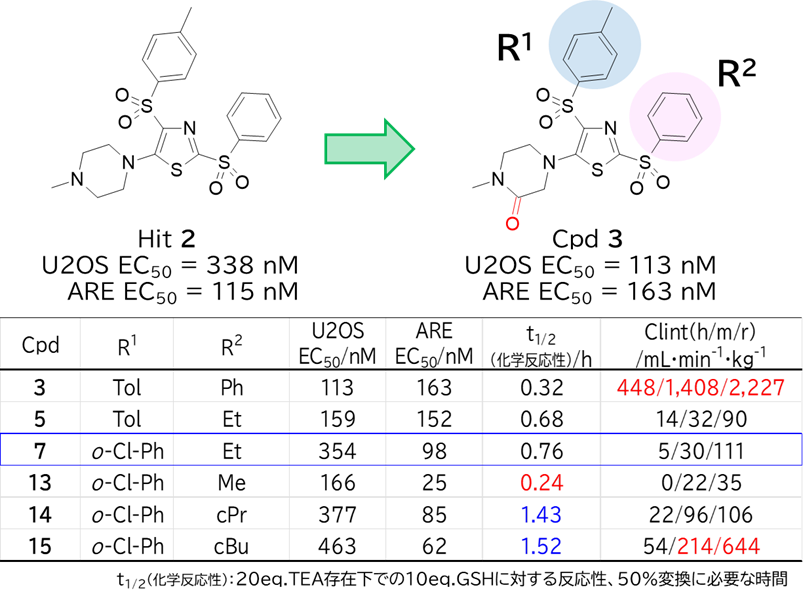
③化合物7のプロファイリングおよび遺伝毒性回避
・in vivo試験:化合物7 (100 mg/kg)をマウスに経口投与してPK/PD評価
✓Cmax = 2.7 μM(30分後)、生体内半減期t1/2 = 1.4 h、ASU = 4.45 μM・h
✓投与後6, 24時間の腎臓中の抗酸化タンパク質Nqo1 mRNA濃度が増加
※バルドキソロン (ARE EC50 = 9.2 nM)の10 mg/kgは化合物7の10 mg/kgよりも肝臓中Nqo1 mRNA発現量が多かった。
・Cerepパネルで36受容体を評価し、オフターゲット活性なし (@10 μM)
・化合物7は遺伝毒性試験でpositive (染色体異常誘発能)
✓エチル基をシクロプロピル基に変えた化合物14はnegative
→残念ながらin vivo試験伸び悩み
✓ピペラジノンにキラルなメチル基を導入した化合物23もnegative
✓僅かな構造変換で遺伝毒性は回避しうる!

【化合物23のプロファイリング】
①化合物23とKEAP1の共結晶X線結晶構造解析
・Cys151はチアゾール2位と共有結合を形成
・His129とHis154はクロロベンゼンを挟み込みながらπ-π相互作用を形成
・Arg135はスルホニル基と弱い水素結合を形成
・Lys150はピペラジノンのカルボニル基と弱い静電相互作用を形成しているかも
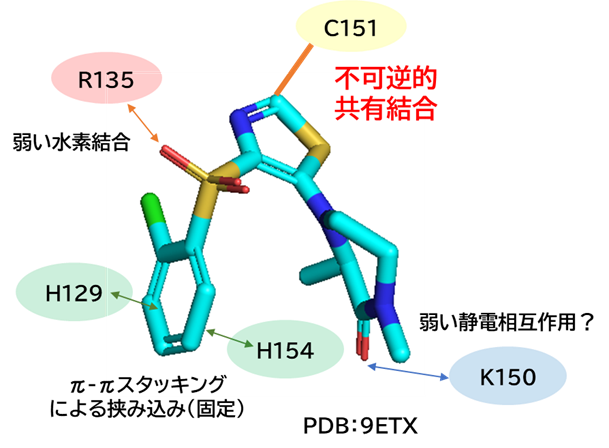
②化合物23の選択性評価
・isoTOP ABPPでCys反応性リガンド結合タンパク質を評価
・化合物23およびネガコン28を3,000以上のタンパク部位と反応させる
✓化合物23は2つのタンパクの3部位が検出(R>4.5)
→RBM12BのCys204、PLIN3のCys39およびCys60
✓化合物28は1つのタンパクの1部位が検出(R>4.5)
→RBM12BのCys204
・示差走査蛍光定量法 (DSF)で96キナーゼを評価し、有意な相互作用なし
・放射性リガンド結合アッセイで45受容体を評価し、最大阻害率31% (@10 μM)
・化合物23は、高い選択性を有する共有結合阻害剤であり、新しいケミカルクラスの共有結合阻害剤として、他の標的タンパク質への適応が期待される。
今回注目したいのは、2点です。
一つ目は、高い選択性です。
化合物23は、isoTOP ABPPで3,000以上のCys反応性リガンド結合タンパク質を評価して2つのオフターゲットタンパク質としか結合しませんでした。これは、共有結合反応基 (warhead)の2-スルホニルチアゾールの反応性が低く、『標的タンパク質にハマった状態でセリンやシステインが近傍にいる』という条件下で反応するためと考えられます。逆に近傍にいないと反応しない、間合いが大事ということでしょう。
そもそも共有結合性キナーゼ阻害剤に頻用されるアクリルアミドも、リガンドが標的タンパク質に結合した際、近くのCysがあると反応する。逆に近傍にいないと反応しづらいため、warheadを付けることでキナーゼ選択性が上がると聞いたことがあります。

反応性と選択性の関係については、九州大学の王子田先生のクロロフルオロアセチル (CFA)基で同様の考察をしており、CFA基が標的タンパク質のポケット内で近接効果が生じたときのみ速やかにチオール基と反応し、近接効果の働かないオフターゲットのチオール基とは反応しにくいことによって選択性が出るとのことです。
コバレント阻害剤の標的特異性向上を目指した新規反応基の探索とEGFR阻害剤への応用
https://www.jstage.jst.go.jp/article/medchem/27/2/27_92/_article/-char/ja/
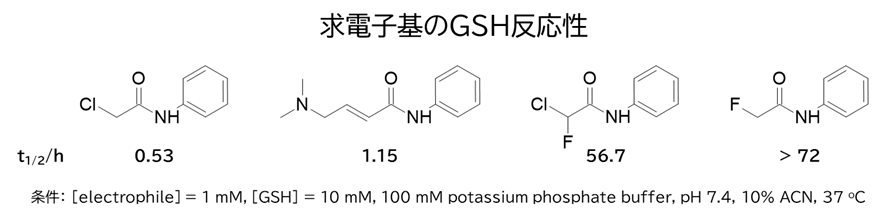
よって、今回の論文でも、t1/2が短いほど選択性は低くなり、長いほど選択性が高くなるかもしれません。合わせて興味深いのは、化合物7のエチル基を小さいメチル基に変換してt1/2が短くなった化合物13はその影響で活性が向上したが、嵩高いcPrやcBuに変換してt1/2が長くなった化合物14, 15は活性が維持されている点です。活性と選択性は必ずしもトレードオフにはならないようです。
二つ目は、2-スルホニルチアゾールがwarheadであることです。
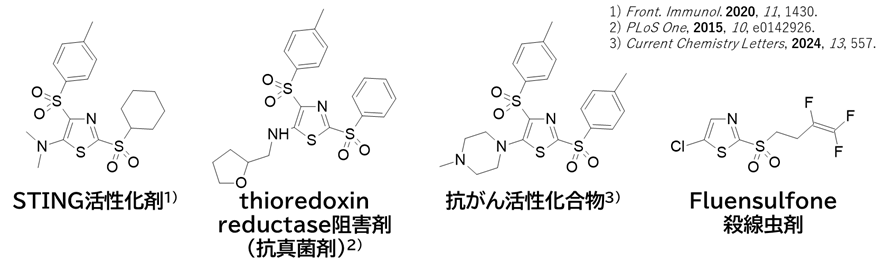
類似構造でSTING活性化剤や抗真菌剤、抗がん活性化合物の報告例がありますが、いずれも共有結合性かどうかの言及はありません。また、2-スルホニルチアゾール構造を持つ化合物としてフルエンスルホンという農薬がありますが、作用機序は不明のようです。
この共有結合性は予測・デザインすることはできるのでしょうか?
何となくJulia-Kocienskiオレフィン化反応の遷移状態と似ているような気がします。

すると、他のJulia試薬 (ピリジンやトリアゾール)も同じように共有結合性が期待できるかもしれません。Nosyl (2-Nitrobenzenesulfonyl)基も近い気がします。すると、アクリルアミドなどwarheadを付ける以外に、有機合成化学の考え方で、化合物の部分骨格に共有結合性を付与する (warheadに変換する)ことで、標的タンパクにハマってCys/Ser残基が近くにある状態でないと反応しない高選択的な共有結合性化合物をデザインすることができるかもしれませんね。ところでEnamine社やAxcelead Drug Discovery Partners社のCovalent Libraryはどんな感じなんでしょう。今回みたいなケミカルクラスも入っているのかな?
いやぁ、メドケムって本当にいいものですね。