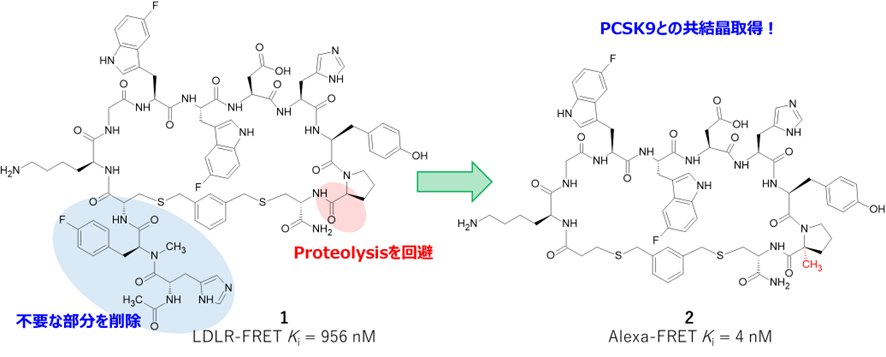
低分子でいく
近年、低分子や抗体以外に様々なモダリティが開発され、それによって狙える標的の幅も大きく広がってきています。環状ペプチドは、抗体に代わって経口投与により細胞内タンパク質間相互作用 (Protein-Protein Interaction, PPI)を阻害するアプローチとして注目されています。とは言え、現状では環状ペプチドの経口投与や細胞膜透過性は容易ではなく、盛んに研究が行われている状況です。一方で、PPIは結合面が平坦で広く柔軟であるため低分子で狙うには難易度が高い標的です。
今回は、日本発のベンチャーPRISM Biolab社によるPPIを標的として取得した環状ペプチドを低分子化するアプローチを紹介します。
別に相手が誰だろうと俺は”ペプチド模倣(低分子)”しか使わない

Rational Strategy for Designing Peptidomimetic Small Molecules Based on Cyclic Peptides Targeting Protein–Protein Interaction between CTLA-4 and B7-1
https://doi.org/10.3390/ph15121506
細胞傷害性Tリンパ球抗原4 (Cytotoxic T Lymphocyte-associated Antigen 4, CTLA-4)、別名CD152は、活性化T細胞や制御性T細胞の表面に発現する免疫調節因子の一つである。抗原提示細胞の一つである樹状細胞上のB7分子 (B7-1およびB7-2)をリガンドとして結合し、T細胞活性化を抑制する。つまり、CTLA-4とB7分子のPPIを阻害することによってT細胞の活性増強および維持が期待される。
以前に、Fragment-based drug discovery (FBDD)の大家であるVanderbilt大学のFesik教授らはFBDDを用いてCTLA-4に結合する低分子を取得したものの、本手法はホットスポットをポイントで狙うアプローチであるため広い結合表面で相互作用するCTLA-4には適さないことが分かった。そこで、PRISM社は、広く作用する環状ペプチドを取得し、それを低分子化するアプローチにチャレンジした。
【ハイライト】
1)ディスプレイ法で環状ペプチド取得、アラニンスキャンで重要残基を抽出
2)Pepmetics骨格にアミノ酸残基を導入して低分子化
3)CTLA-4-B7-1複合体結晶情報を元にSBDDで活性43倍向上
【その1:ディスプレイ法で環状ペプチド取得、アラニンスキャンで重要残基を抽出】
- 無細胞タンパク質合成キットPUREfrexⓇを用いて環状ペプチドをスクリーニング。
- PUREfrexⓇはジーンフロンティア社と東京大学の上田卓也教授が共同開発https://www.genefrontier.com/solutions/purefrex/
- 環状ペプチドライブラリーは、12個のランダムなアミノ酸で構成
- 12 merペプチドの両端にCysを入れてS-S結合で環構築 (合計14 mer)
- Cysの先にそれぞれGlyが2つ繋がり、N末はFLAG, C末はc-Myc, tolAスペーサー, secMが続く
- ビオチン化CTLA-4-Fcを用いてスクリーニング
- カウンター系は、ビオチン化ヒトIgG1-Fc
- CTLA-4に特異的に結合する環状ペプチドを7つ取得。
- ペプチドC4-302 (配列:GGCMHPFLLVVSHHFCGG)はCTLA-4に結合、ヒトFcに結合せず
- ※CCでS-S結合を形成、GGはリンカー
- 残りの6ペプチドはCTLA-4とヒトFcの両方に結合のためボツ
- C4-302はCTLA-4とリガンドB7-1のタンパク質間相互作用を阻害
- C4m-3127のCTLA-4に対する結合親和性はEC50 = 0.0747 μMで、元のC4-302から52倍向上
- CTLA-4-ビオチン化B7-1評価系で阻害活性 (IC50 = 11.5 μM)確認
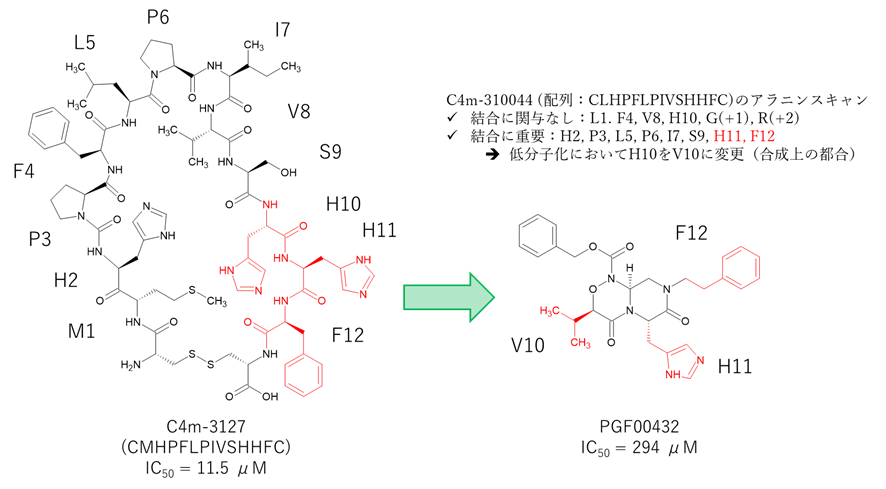
- C4m-3127の類似ペプチドC4m-310044 (配列:GGCLHPFLPIVSHHFCGR, EC50 = 0.0818 μM)を親配列としてアラニンスキャンを実施
- 結合に関与なし: F4, V8, H10, G(+1), R(+2)
- 結合に重要:H2, P3, L5, P6, I7, S9, H11, F12
- H2, P3, L5, S9, H11, F12はCTLA-4との結合に必須
- P6はL, R, Qに、I7はV, T, Lに置換可能
- 2残基は結合には関与していないが結合親和性に寄与している
【その2:Pepmetics骨格にアミノ酸残基を導入して低分子化】
- ペプチド模倣技術 (Pepmetics)を用いてはC4m-3127の低分子化を実施
- 独自の骨格 (scaffold)に3~5個の置換基を導入した化合物ライブラリー
- 置換基の位置が短鎖α-helix, β-turn構造の安定配座を模しているhttps://prismbiolab.com/ja/technology/peptide-mimetics/
- C4m-3127の12 mer (MHPFLPIVSHHF)の3つの連続するアミノ酸残基をPepmetics骨格に導入した化合物を順次合成
- プロリン模倣の制限のため(M1, H2, P3), (H2, P3, F4), (F4, L5, P6), (L5, P6, I7)は合成せず
- 連続するH10, H11は合成上の制限によりH10をV10に変更
※C4m-310044のアラニンスキャンでH10は結合に関与無し、H11は結合に必須
- PGF00432 (V10, H11, F12)を取得
- CTLA-4-ビオチン化B7-1評価系で阻害活性 (IC50 = 294 μM)あり
【その3:CTLA-4-B7-1複合体結晶情報を元にSBDDで活性43倍向上】
- PGF00432とCTLA-4のドッキングシミュレーションを実施
- CTLA-4-B7-1複合体結晶情報 (PDB: 1I8L)を使用
- 親ペプチドC4-302がCTLA-4とB7-1の相互作用を阻害した結果からPGF00432もその相互作用面に結合して阻害していると仮定
- PGF00432のヒスチジン残基はCTLA-4のGlu48と相互作用
- 強塩基のグアニジンに変換して相互作用の増強を狙う
- PGF00432のバリン残基はCTLA-4のIle93/Leu39の疎水性ポケットを部分的に占有
- 疎水性が高くサイズの大きいシクロヘキサンに変換して疎水性ポケットを埋める
- PGF00432のフェニルアラニン残基はCTLA-4-B7-1作用面 (溶媒領域)に位置
- ( 図8Bを見るとTyr104とスタッキングしているように見えるが違う?)
- 嵩高い置換基に変換してCTLA-4-B7-1作用面で立体障害を狙う
- CTLA-4-B7-1複合体結晶情報 (PDB: 1I8L)を使用
- PGF00506 (IC50 = 6.8 μM)を取得
- PGF00432と比べて43倍向上、C4m-3127の2倍弱の阻害活性

今回注目したいポイントは2つあります。
一つ目は、低分子の取得にX線結晶構造解析を必要としなかったことです。
ディスプレイ法で取得した環状ペプチドの3つの連続するアミノ酸残基をPepmetics骨格に導入し、順次合成した結果、PGF00432が見出されました。また、ペプチドのアラニンスキャンで重要残基を抽出することで、H10をV10に変換しています。ペプチドさえあれば結晶が取れなくても低分子化を狙えるのは非常に有用です。
二つ目は、低分子に極性アミノ酸と芳香族アミノ酸が含まれていることです。
過去に紹介した中外さんのOrforglipronや塩野義さんのCompound 14にも極性アミノ酸と芳香族アミノ酸が含まれています。
※ただし、OrforglipronがGLP-1ペプチドから低分子化したかもというのは個人的な推理によるもの(以下記事参照)で実際は違うかも・・・違ったらすみません。
中外さん:https://azarashi-panda.hatenablog.com/entry/2023/01/02/082956
塩野義さん:https://azarashi-panda.hatenablog.com/entry/2022/12/10/054513

低分子で結合面が平坦で広く柔軟なPPIを狙おうとしたら、極性アミノ酸による標的タンパクとの水素結合のようなエンタルピー駆動型の相互作用が重要かもしれません。塩野義さんの例ではHxG5とW6によるInduced fitが起こったため、芳香族性アミノ酸にはそのような作用も期待できるかも。
ペプチドライブラリーは極性アミノ酸や芳香族性アミノ酸にフォーカスしてデザインするのが効果的でしょう。芳香環にはハロゲン(特にフッ素)を入れても良いかな。
(ここまできたらペプチドの低分子化せずに直接Pepmetics骨格にフォーカスした置換基を導入した化合物ライブラリーでスクリーニングした方が早いかもしれないけど。)
そう言えば、中外さんの膜透過性ペプチドのライブラリーは『電荷を持つアミノ酸を排除して、疎水性アミノ酸』で構成されていました。
中外さん:https://azarashi-panda.hatenablog.com/entry/2023/11/30/055443
上記の話で言うと、中外さんの膜透過性ペプチドは低分子化が難しい・・・と言うか、相互作用も疎水性相互作用を中心としたエントロピー駆動型でしょうから異なるし、もし結合部位・結合様式も異なるなら、適した標的タンパクも異なるかもかもしれないので、お互いに棲み分け・使い分けが出来るかもしれません。
ところで、PGF00432 (IC50 = 294 μM)から誘導されたPGF00506 (IC50 = 6.8 μM)は元のペプチドC4m-3127 (IC50 = 11.5 μM)より強い阻害活性を持っているとは言え、マイクロオーダーで物足りないです。低分子でPPIを阻害するにはこれが限界なのか?個人的には共有結合官能基に期待しています。K-RAS阻害剤において、システインを狙った共有結合官能基(warhead)が導入された化合物がありますが、いつも都合よく傍にシステインがあるとは限らないので、他の官能基も狙えたら良いよね、リジンとか。
フェェェェドインッ!!