結合が裏返る
近年、シミュレーション技術の発展は凄まじく、バーチャルスクリーニングのみで短期間かつ高確率で活性化合物を取得できるようになりつつあります。一方で、実際にX線結晶構造解析で確認したら、思ってたんと違う・・・あると思います。
今回は、Novartis社と大正製薬、それぞれ実際にX線結晶構造解析で確認したら結合様式が予想外に反転していた事例を紹介します。
結合様式が・・・裏返るッッ

【ハイライト】
1)シミュレーションとX線結晶構造解析で結合様式が180°反転(Novartis)
2)X線結晶構造解析を元に芳香環を導入して新規相互作用獲得、活性激増(Novartis)
3)六員環ピペリジンを七員環アゼピンに変換すると結合様式が180°反転(大正製薬)
4)X線結晶構造解析を元にアミノ基を導入して新規相互作用獲得、活性向上(大正製薬)
Novartis社の事例(ペプチドリーム舛屋さん)
Discovery of dihydroisoquinolinone derivatives as novel inhibitors of the p53–MDM2 interaction with a distinct binding mode
https://doi.org/10.1016/j.bmcl.2015.06.058
p53は腫瘍抑制因子として細胞ががん化するとアポトーシス誘導して除去する働きを持つ。一方、MDM2はp53と相互作用してその機能を抑制することから、p53-MDM2タンパク質間相互作用を阻害する化合物は、抗がん剤として期待される。
Novartis社は、以前にp53から誘導されたペプチドとMDM2のX線結晶構造解析を元に、ペプチドのPhe19, Trp23, Leu26がMDM2との相互作用に必須なファーマコフォアとして抽出し、それら3つのアミノ酸残基が占有する3つのサブポケットの中央に位置するMDM2のVal93残基との相互作用をベースに化合物をデザインする『セントラルバリンコンセプト』を提案し、複数のp53-MDM2タンパク質間相互作用阻害剤を創出してきた。今回、過去研究を元にバーチャルシミュレーションを駆使して新規ケミカルクラスの取得を目指した。
【その1:シミュレーションとX線結晶構造解析で結合様式が180°反転】
- Novartis社5,000化合物のバーチャルスクリーニングで化合物1を取得
- TR-FRETアッセイでIC50 = 0.54 μM
- セントラルバリンコンセプトに基づいた相互作用を予測
- 過去研究のSAR情報を元に誘導体展開したが活性向上せず
- 溶解性タグを付けた化合物5でMDM2との共結晶取得
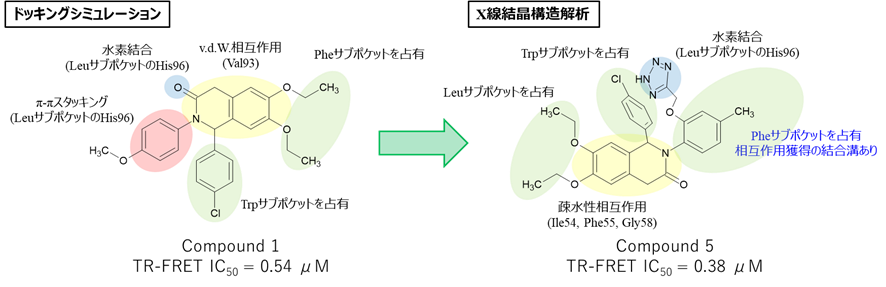
【その2:X線結晶構造解析を元に芳香環を導入して新規相互作用獲得、活性激増】
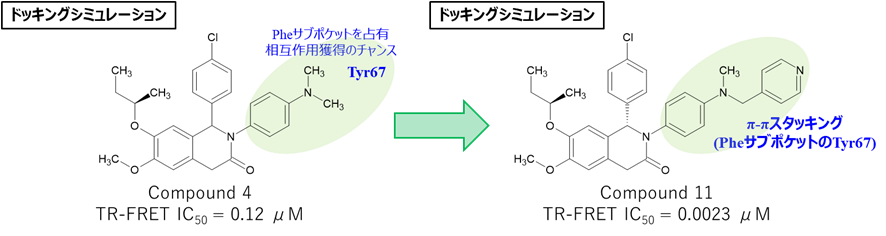
- 化合物4のジメチルアミノフェニル基が占有するPheサブポケットに注目
- PheサブポケットのTyr67と相互作用を狙う
- メチル基をピリジルメチル基に変換した化合物11 (IC50 = 0.0023 μM)を合成
- 導入したピリジン環がMDM2のTyr67残基とπ-πスタッキングを形成
- 化合物11は化合物4 (IC50 = 0.12 μM)と比べて活性が50倍以上向上
大正製薬の事例
Discovery of novel indole derivatives as potent and selective inhibitors of
proMMP-9 activation
https://doi.org/10.1016/j.bmcl.2023.129541
Matrix MetalloProteinase-9 (MMP9)は、活性中心に亜鉛を持つエンドペプチダーゼである。フラジャイルX症候群や自閉症スペクトラム症の患者においてMMP9の発現増加が確認されており、MMP9の発現増加は、神経細胞の樹状突起スパイン形成異常を引き起こす原因として、それら疾患との関与が示唆されている。
古典的なMMP阻害剤は活性中心の亜鉛に強く配位するヒドロキサム酸を持ち、非常に高活性だがMMP間の選択性が低く、副作用の懸念がある。それに対して近年、ヤンセンファーマからproMMP9から活性化MMP9への変換を阻害するJNJ0966が報告された。JNJ0966が結合しているアロステリック部位は他のMMPファミリーとの相同性が比較的低いため選択性の改善が期待できる。
大正製薬は、JNJ0966と同様にアロステリック部位に結合してproMMP9活性化を阻害する化合物の取得を目指した。
【その3:六員環ピペリジンを七員環アゼピンに変換すると結合様式が180°反転】
- 自社ライブラリーを用いたHTSで化合物1を取得
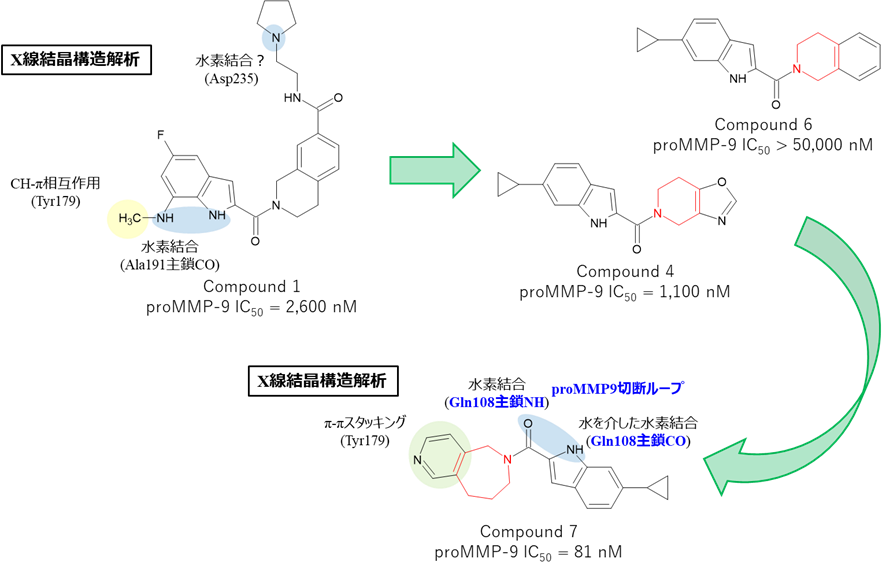
【その3:X線結晶構造解析を元にアミノ基を導入して新規相互作用獲得、活性向上】
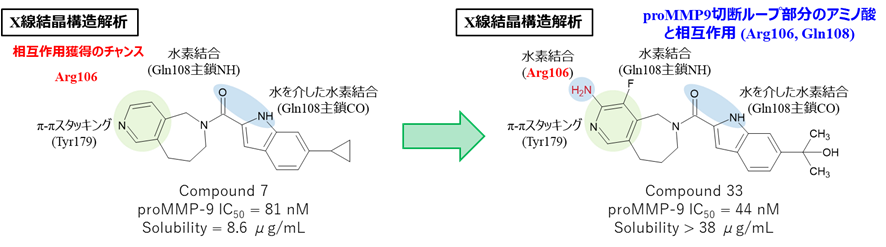
- 化合物7のピリジン環周辺のArg106に注目
- Arg106はproMMP9活性化の際に切断されるループの一部
- 水素結合ドナーを導入してArg106主鎖COと相互作用して活性向上を狙う
- アミノ基を導入して相互作用獲得を狙いつつ、フルオロ基で水素結合ドナーを一つマスク
- カルボキシ基を導入してArg106残基と相互作用したら活性向上は期待できるが脳内移行性が悪くなる?
- アミノ基を導入した化合物33 (IC50 = 41 nM)を合成
- 導入したアミノ基がArg106主鎖COと水素結合を形成
- 化合物33は化合物7と比べて活性が2倍向上
今回注目したいポイントは2つあります。
一つ目は、やはりX線結晶構造解析での確認は重要であるということです。特にSARが予測通り説明できない場合は結合様式が予測と異なる場合があります。また、環変換や置換基導入がきっかけで結合様式が変わる場合もあるため、ヒット化合物やリード化合物一つ構造解析すれば十分ッ!ではなく、ポイントポイントで確認した方が良いです。構造解析の情報が増えることでシミュレーションの精度も上がりますし。
・・・と簡単に言いますが、SAR説明が難しい創薬プロジェクトに限って膜タンパクとか結晶取得が難しい標的だったりするんですよね・・・ここでCryo-EMが活躍するのかな。あとNovartis社の論文にあったように化合物の溶解性は絶対必須。
二つ目は、大正製薬の事例において、活性激増で新規獲得した相互作用は『proMMP9活性化の際に切断されるループの一部』でした。もしかしてアミノ酸残基より主鎖と相互作用したのが良かったのかも? それは置いといて、活性を上げるための新規相互作用はどこでも良い訳ではなくて、どのアミノ酸と相互作用するかが重要です。たくさん相互作用を狙って化合物に置換基を導入しまくれば、それだけ分子サイズが大きくなって溶解度や細胞膜透過性など他のプロファイルに悪影響を及ぼします。
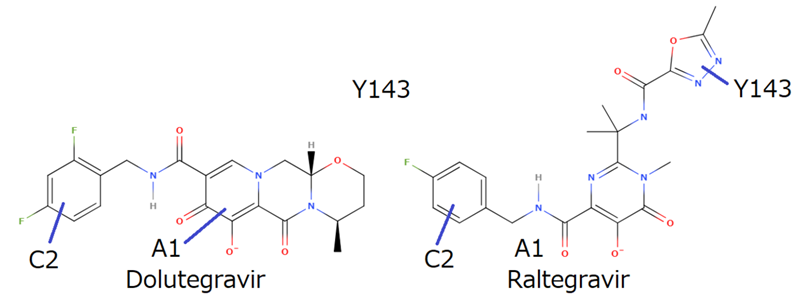
必要な相互作用だけで小さく強く効かせるコンセプトは、以前に塩野義さんのドルテグラビルが耐性株に効かす(もしくは耐性化を防ぐ)重要なポイントであるかもと紹介しました。メドケムデザインはミニマリストであるべきなのかも。
https://azarashi-panda.hatenablog.com/entry/2022/12/19/062129
小さく打とう、小さく打とう、とすると大きく飛ぶんです。